Desintegración Radiactiva. Grupo 27 C
| Trabajo realizado por estudiantes | |
|---|---|
| Título | DESINTEGRACIÓN RADIACTIVA. GRUPO 27 C |
| Asignatura | Ecuaciones Diferenciales |
| Curso | Curso 2014-15 |
| Autores | Pablo Goenechea Álvarez
Íñigo Uraga Palacio Paula de Santos Muñoz Ignacio Lizasco Casillas |
| Este artículo ha sido escrito por estudiantes como parte de su evaluación en la asignatura | |
El Trabajo 3 del curso 2014/2015 de Ecuaciones Diferenciales nos habla del comportamiento de distintos materiales radiactivos (durante gran parte del trabajo será el isótopo [math] C^{14} [/math]). El cual se desintegra de forma natural para formar elemento o isótropo del mismo elemento con una rapidez proporcional a la cantidad de material radiactovo presente. Este procedimiento puede simularse con la siguiente ecuación diferencial para la concentración de elemento radiactivo: :[math] M'(t)=-kM(t) [/math] A partir de esto tendremos que ir resolviendo los problemas que nos plantea el trabajo y que son los que se pueden ver en el índice del contenido:
Contenido
- 1 ) Interpretación
- 2 ) Cálculo de la Edad con el Método Euler
- 3 ) Cálculo de la Edad con el Método del Trapecio
- 4 ) Cálculo de la Vida Media con el Método Runge-Kutta
- 5 ) Determinación el Sistema de Ecuaciones Diferenciales
- 6 ) Resolución del PVI con Método Euler y Método del Trapecio
- 7 ) Resolución del PVI con las Constantes Cambiadas
1 ) Interpretación
M(t) es una función que depende del tiempo y mide la concentración de la sustancia A, su derivada M'(t) mide la velocidad de desintegración de A en favor de B y es proporcional a "k" que es la constante de desintegración del material radiactivo (negativa en este caso puesto que decrece la concentración de A). La concentración de B será 1-M(t) puesto que la concentración de A más la concentración de B es siempre igual a 1.
2 ) Cálculo de la Edad con el Método Euler
En este apartado se pide carcular la edad de unos restos arqueológicos sabiendo que contiene un 8% de [math] C^{14} [/math] del que se encuentra en un ser vivo y teniendo en cuenta que podemos tomar la diferencia de contenido en [math] C^{14} [/math] del hueso antiguo debida únicamente a su desintegración. Para este cálculo nos dan una [math] k=1.24x10^{-4} [/math] y tenemos que hacerlo con dos pasos intermedios, h1=0.1 y h2=0.01. Además nos preguntan si es "estable".
% Condiciones Iniciales
t0=0;
y0=1;
h1=0.1;
y1(1)=y0;
t1(1)=t0;
i=1;
k=1.24e-04;
% Primer Programa (h=0.1)
while y1(i)>0.08;
y1(i+1)=y1(i)+h1*(-k*y1(i));
t1(i+1)=t1(i)+h1;
i=i+1;
end
% Recalculamos las Condiciones Iniciales
t0=0;
y0=1;
h2=0.01;
y2(1)=y0;
t2(1)=t0;
n=1;
k=1.24e-04;
% Segundo Programa (h=0.01)
while y2(n)>0.08;
y2(n+1)=y2(n)+h2*(-k*y2(n));
t2(n+1)=t2(n)+h2;
n=n+1;
end
% Resultados y Gráficas con ambos pasos intermedios
disp('años de antiguedad de los huesos (h=0.1)')
disp (t1(i))
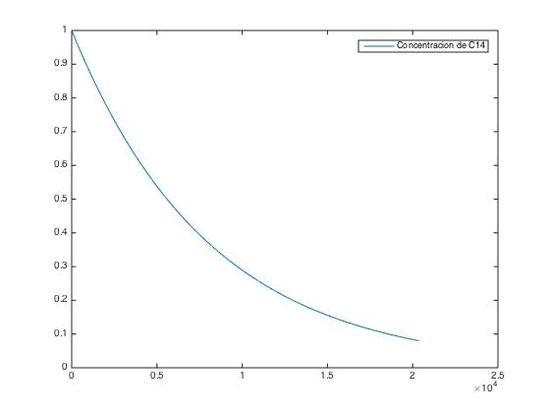
figure(1)
plot(t1,y1)
legend('Concentración de C14')
disp('años de antiguedad de los huesos (h=0.01)')
disp(t2(n))
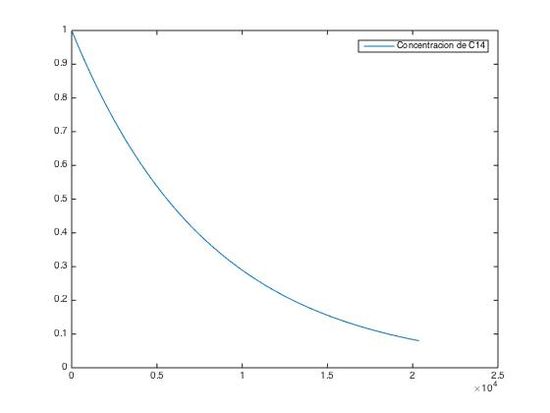
figure(2)
plot(t2,y2)
legend('Concentración de C14')
Años de antiguedad de los huesos (h=0.1) = 20369 años.
Años de antiguedad de los huesos (h=0.01) = 20369 años.
Como se puede ver en los resultados, el método es estable, puesto que da el mismo resultado para ambos pasos.
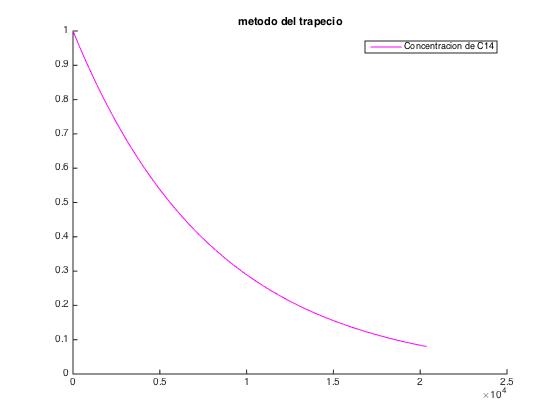
3 ) Cálculo de la Edad con el Método del Trapecio
Ahora nos piden repetir el apartado anterior pero utilizando el método del Trapecio con una h=0.1, realizando el programa de forma que se pare cuando se alcance el 8% de la cantidad inicial.
% Condiciones Iniciales
t0=0;
h1=0.1;
y0=1;
y(1)=y0;
t1(1)=t0;
i=1; n=1; k=1.24e-04;
% Programa
while y(i)>y0*0.08;
y(i+1)=((1-h1*k/2)/(1+h1*k/2))*y(i);
t1(i+1)=t1(i)+h1;
i=i+1;
end
% Resultados y gráfica
disp('tiempo final:')
disp(t1(end))
disp(i)
hold on
plot(t1,y,'m')
title('metodo del trapecio')
legend('Concentracion de C14')
hold offAños de antiguedad de los huesos = 20369 años.
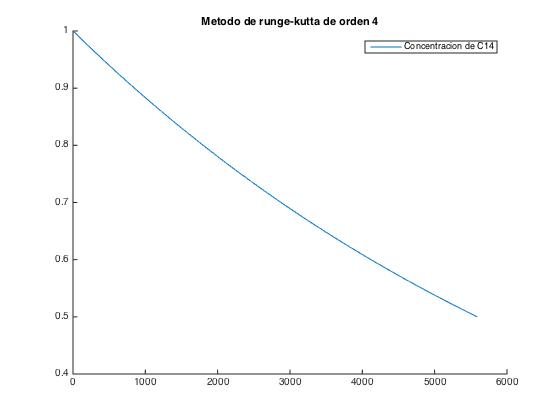
4 ) Cálculo de la Vida Media con el Método Runge-Kutta
Aquí el enunciado pide calcular, empleando el método Runge-Kutta de cuarto orden, la "vida media" que no es otra cosa que el tiempo que tarda en reducirse a la mitad un elemento radiactivo.
% Condiciones Iniciales
t0=0;
h=0.1;
M0=1;
t(1)=t0;
M(1)=M0;
k=1.24e-04;
i=1;
% Programa
while M(i)>0.5;
K1=-k*M(i);
t2=t(i)+(h/2);
K2=-k*(M(i)+(h/2)*K1);
t3=t2;
K3=-k*(M(i)+(h/2)*K2);
K4=-k*(M(i)+h*K3);
M(i+1)=M(i)+(h/6)*(K1+2*K2+2*K3+K4);
t(i+1)=t(i)+h;
i=i+1;
end
% Resultados y gráfica
disp('Tiempo medio: ')
disp(t(end))
hold on
plot(t,M)
title('Metodo de runge-kutta de orden 4')
legend('Concentracion de C14')
hold off
5 ) Determinación el Sistema de Ecuaciones Diferenciales
El sistema de ecuaciones tendrá tres ecuaciones independientes a resolver, una para cada sustancia: A, B y C. La derivada de cada sustancias respecto del tiempo mide la velocidad de desintegración de la sustancia en cuestión y es representada por A', B' y C'.
Como la sustancia A se desintegra en B, la constante (k1) será negativa puesto que decrece la concentración de A. La sustancia B crece al mismo ritmo que la velocidad de desintegración de A por lo que k1 será positiva pero a la vez se desintegra en favor de C a una velocidad de k2 por su concentración, siendo k2 negativa. Por último, la sustancia C crecerá al ritmo de la desintegración de B, siendo esta velocidad igual a k2 (positivo) por la concentración de B.
El sistema quedará de la siguiente forma:
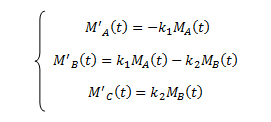
6 ) Resolución del PVI con Método Euler y Método del Trapecio
En este apartado, el trabajo nos pide hayar las concentraciones de las sustancias A, B y C en función del tiempo. Las concentraciones iniciales serán: A0=1, B0=0, C0=0. Las constantes de desintegración serán respectivamente k1=5 y k2=1. Para ello utilizaremos los métodos de Euler y del Trapecio con un paso intermedio h=0.1 y un tiempo comprendido entre 0 y 10 años.
% Condiciones Iniciales del PVI
t0=1; A0=1; B0=0; C0=0; h=0.1;
A(1)=A0;
B(1)=B0;
C(1)=C0;
t(1)=t0;
i=1; n=1; k1=5; k2=1;
% MÉTODO DE EULER
while t<10
A(i+1)=A(i)+h*(-k1*A(i));
B(i+1)=B(i)+h*(k1*A(i))+h*(-k2*B(i));
C(i+1)=C(i)+h*(k2*B(i));
t(i+1)=t(i)+h;
i=i+1;
end
% Hacemos la gráfica
figure(1)
hold on
plot(t,A)
plot(t,B,'g')
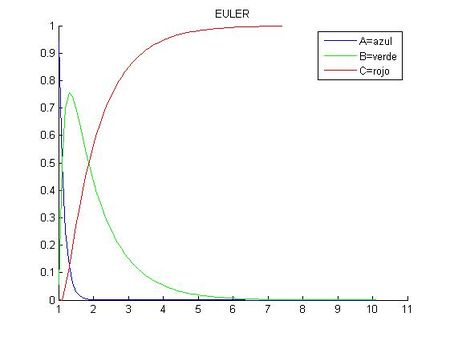
plot(t,C,'r')
title('EULER')
legend('A=azul','B=verde','C=rojo')
hold off
%MÉTODO DEL TRAPECIO
% Renombramos las condiciones iniciales
a0=1; b0=0; c0=0;
a(1)=a0; b(1)=b0 ;c(1)=c0;
t1(1)=t0;
while t1(i)<10
a(i+1)=((2-h*k1)/(2+h*k1))*a(i);
b(i+1)=b(i)*((2-h*k2)/(2+h*k2))+(h*k1/(2+h*k2))*(a(i)+a(i+1));
c(i+1)=c(i)+(h*k2/2)*(b(i)+b(i+1));
t1(i+1)=t1(i)+h;
i=i+1;
end
% Hacemos la Gráfica
figure(2)
hold on
plot(t1,a)
plot(t1,b,'g')
plot(t1,c,'r')
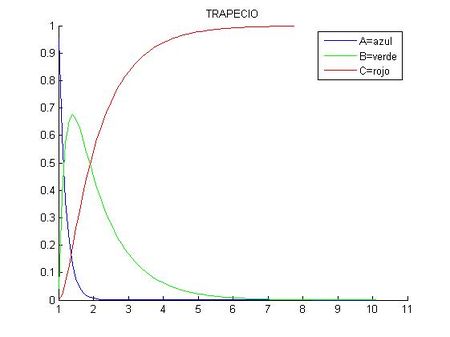
title('TRAPECIO')
legend('A=azul','B=verde','C=rojo')
hold offComo se puede observar en las gráficas, al ser la constante de desintegración de A (k1) muy alta y la de B (k2) más baja, la sustancia A se desintegra rápidamente, mientras la B crece hasta que su concentración es cinco veces la de A, entonces empieza a decrecer según va apareciendo C. También se ve que ambas gráficas difieren ligeramente debido a que siempre se produce un error, y en el caso del método del trapecio, este error es menor al ser un método más exacto, por lo que podría decirse que la gráfica de la derecha es más exacta.
7 ) Resolución del PVI con las Constantes Cambiadas
En este apartado, el trabajo nos pide hayar las concentraciones de las sustancias A, B y C en función del tiempo. Las concentraciones iniciales serán: A0=1, B0=0, C0=0. Las constantes de desintegración serán respectivamente k1=1 y k2=5 (al contrario que en el apartado anterior). Para ello utilizaremos los métodos de Euler y del Trapecio con un paso intermedio h=0.1 y un tiempo comprendido entre 0 y 10 años.
% Condiciones Iniciales del PVI
t0=1; A0=1; B0=0; C0=0; h=0.1;
A(1)=A0;
B(1)=B0;
C(1)=C0;
t(1)=t0;
i=1; n=1; k1=1; k2=5;
% MÉTODO DE EULER
while t<10
A(i+1)=A(i)+h*(-k1*A(i));
B(i+1)=B(i)+h*(k1*A(i))+h*(-k2*B(i));
C(i+1)=C(i)+h*(k2*B(i));
t(i+1)=t(i)+h;
i=i+1;
end
% Hacemos la gráfica
figure(1)
hold on
plot(t,A)
plot(t,B,'g')
plot(t,C,'r')
title('EULER')
legend('A=azul','B=verde','C=rojo')
hold off
%MÉTODO DEL TRAPECIO
% Renombramos las condiciones iniciales
a0=1; b0=0; c0=0;
a(1)=a0; b(1)=b0 ;c(1)=c0;
t1(1)=t0;
while t1(i)<10
a(i+1)=((2-h*k1)/(2+h*k1))*a(i);
b(i+1)=b(i)*((2-h*k2)/(2+h*k2))+(h*k1/(2+h*k2))*(a(i)+a(i+1));
c(i+1)=c(i)+(h*k2/2)*(b(i)+b(i+1));
t1(i+1)=t1(i)+h;
i=i+1;
end
% Hacemos la gráfica
figure(2)
hold on
plot(t1,a)
plot(t1,b,'g')
plot(t1,c,'r')
title('TRAPECIO')
legend('A=azul','B=verde','C=rojo')
hold off
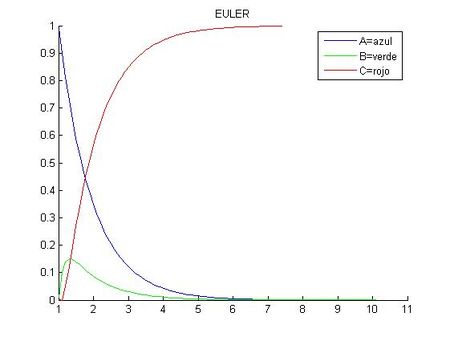
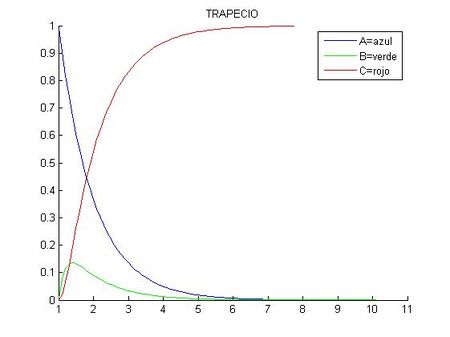 En este caso, las constantes han cambiado, por lo que A se desintegra lentamente a B. Mientras que B apenas crece puesto que su velocidad de desintegración es mucho mayor que la de A (empieza a decrecer cuando la concentración de A es cinco veces la suya). A su vez, C crece rápidamente conforme va apareciendo la sustancia B.
Lo que es igual al apartado anterior es la diferencia de las gráficas siendo más aproximada la de la derecha (correspondiente al método del Trapecio).
En este caso, las constantes han cambiado, por lo que A se desintegra lentamente a B. Mientras que B apenas crece puesto que su velocidad de desintegración es mucho mayor que la de A (empieza a decrecer cuando la concentración de A es cinco veces la suya). A su vez, C crece rápidamente conforme va apareciendo la sustancia B.
Lo que es igual al apartado anterior es la diferencia de las gráficas siendo más aproximada la de la derecha (correspondiente al método del Trapecio).