Reacciones complejas (Grupo D1)
| Trabajo realizado por estudiantes | |
|---|---|
| Título | Reacciones complejas (Grupo D1) |
| Asignatura | Ecuaciones Diferenciales |
| Curso | Curso 2014-15 |
| Autores | Rincón Crespo, Kevin
Rodríguez Gómez, Javier Sans Jiménez, Alejandro Sesto Muñoz, María Victoria Vallejo Asín, José Manuel Villarino Redondo, Álvaro |
| Este artículo ha sido escrito por estudiantes como parte de su evaluación en la asignatura | |
Contenido
1 Introducción
Se considera una reacción química irreversible en una solución bien mezclada. Supondremos que la reacción ocurre para un volumen y temperatura constantes. Al inicio se encuentran dos reactivos A y B, que van formando un producto C en lo que se conoce como una reacción bimolecular, es decir, una molécula de A y una de B producen una de C,
A + B → C
Supondremos también que se satisface la ley de acción de masas, que establece que la velocidad de reacción es proporcional al producto de las concentraciones de los reactivos.
2 Concentración del reactivo C a lo largo del tiempo
En primer lugar, suponiendo que la reacción es irreversible, es decir, que C no puede volver a formar A y B, se puede expresar la situación mediante el siguiente problema de valor inicial: {█(y^' (t)=k_1 (a_0-y(t) )(b_0-y(t) )@y(0)=0)┤ , t>0
Donde a_0 y b_0 representan las concentraciones iniciales de A y B respectivamente y k1 es la constante de proporcionalidad que indica la ley de acción de masas. y’(t) representa la velocidad de reacción, es decir, la velocidad con que se forma el producto C; mientras que la solución de la ecuación diferencial, y(t), representa la concentración de C, la cantidad de compuesto que se ha formado. Para comprobar que la solución de este problema de Cauchy es única, comenzamos definiendo:
Observamos que f(t,y) es continua en el intervalo I=(0,∞)∩B((0,0),r>0), por lo que ya aseguramos la existencia de al menos una solución. Examinando la derivada parcial:
se deduce que al ser un polinomio no va a haber problemas de continuidad para ninguna bola. De esta forma, podemos asegurar que existe una única solución. Ahora bien, ¿qué pasaría si la reacción fuese reversible? Con esto lo que queremos indicar es que además de formarse C, este también se descompone de nuevo en A y B. Por lo tanto, nos quedaría una ecuación diferencial con la siguiente forma:
Si nos fijamos, la modificación es sencillamente restar y(t) multiplicada por una constante, la cual refleja qué porcentaje de C se va descomponiendo a medida que se da, simultáneamente, la reacción A + B → C. Sin embargo, esta constante no puede tener cualquier valor, ya que en una reacción se cumple la conservación de masa. Por ello, a C le asociaremos el siguiente dominio:
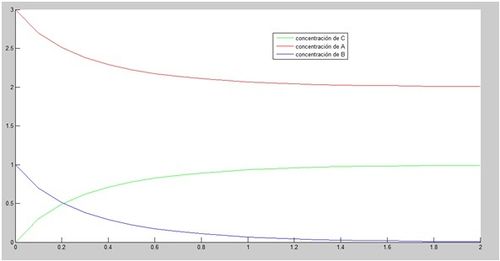
Obsérvese que C tiene que ser mayor que 0 para que sea reversible, pero al mismo tiempo inferior que 1, ya que si no se estaría descomponiendo más compuesto C del que realmente se ha formado, en otras palabras, estaría apareciendo masa de la nada. Una vez llegados a este punto, se procede a ver una interpretación gráfica de la reacción. Para ello, se refleja en la gráfica (en un intervalo de 2 segundos), cómo varían las concentraciones tanto de A (a_0=3 mol/L) y B (b_0=1 mol/L) como de C, para una k_1=1 mol/s. Se comienza, por el momento, aplicando el método de Euler. Posteriormente se utilizarán métodos más precisos.
2.1 Concentración del reactivo C a lo largo del tiempo en un proceso reversible
3 Método de Euler Y Método del Trapecio
4 Método de Runge-Kutta
5 Reacción consecutiva
Consideramos la reacción A + B → k1C → k2D
Para resolverla creamos el sistema siguiente:
[math]y'\ltsub\gt1\lt/sub\gt(t)=k\ltsub\gt1\lt/sub\gt(a\ltsub\gt0\lt/sub\gt − y\ltsub\gt1\lt/sub\gt(t))(b\ltsub\gt0\lt/sub\gt − y\ltsub\gt1\lt/sub\gt(t))[/math]
[math]y'\ltsub\gt2\lt/sub\gt(t)=k\ltsub\gt2\lt/sub\gty\ltsub\gt1\lt/sub\gt(t)[/math]
[math]y\ltsub\gt1\lt/sub\gt(0)=0, y\ltsub\gt2\lt/sub\gt(0)=0[/math]
5.1 La reacción D es más rápida que la reacción C
Tomamos como k1=5, y k2=1; de esta manera la segunda reacción es mucho mas rapido. El tamaño de paso introducido es de h=0.01. Creamos el siguiente código de MatLAB, utilizando los métodos de Euler y de Runge-Kutta:
% apartado 7
clear all
%datos
h=input('Introducir tamaño de paso');
y0=[0;0];
z0=[0;0];
t0=0;
tN=10;
%Definimos la variable independiente t
t=t0:h:tN;
%Creamos la matriz de las soluciones para el método de Euler
y=zeros(2,length(t));
y(:,1)=y0;
%Creamos la matriz de las soluciones para el método de Runge-Kutta
z=zeros(2,length(t));
z(:,1)=y0;
for i=1:length(t)-1
%euler
y(:,i+1)=y(:,i)+h*[1*(3-y(1,i))*(1-y(1,i)); 5*(y(1,i)-y(2,i))];
%runge-kutta
K1=[1*(3-z(1,i))*(1-z(1,i)); 5*(z(1,i)-z(2,i))];
K2=[1*(3-(z(1,i)+h/2*K1(1)))*(1-(z(1,i)+h/2*K1(1))); 5*((y(1,i)+h/2*K1(2))-(y(2,i)+h/2*K1(2)))];
K3=[1*(3-(z(1,i)+h/2*K2(1)))*(1-(z(1,i)+h/2*K2(1))); 5*((y(1,i)+h/2*K2(2))-(y(2,i)+h/2*K2(2)))];
K4=[1*(3-(z(1,i)+h*K3(1)))*(1-(z(1,i)+h*K3(1))); 5*((y(1,i)+h*K3(2))-(y(2,i)+h*K3(2)))];
z(:,i+1)=z(:,i)+h/6*(K1+2*K2+2*K3+K4);
end
figure(1)
hold on
plot(t,y(1,:)) %Concentración de C por Euler
plot(t,y(2,:),'r') %Concentración de D por Euler
plot(t,z(1,:),'k') %Concentración de C por Runge-kutta
plot(t,z(2,:),'g') %Concentración de D por Runge-kutta
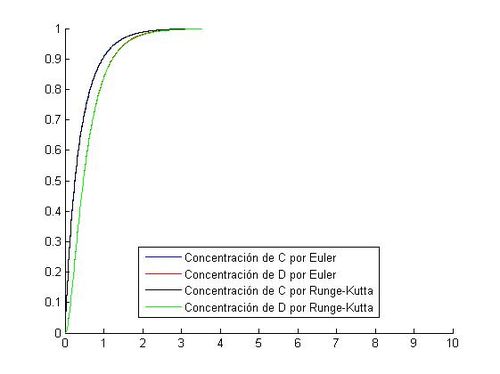
legend('Concentración de C por Euler','Concentración de D por Euler','Concentración de C por Runge-Kutta','Concentración de D por Runge-Kutta','Location','best')
hold offAplicando un paso de 0.01, la grafica de las reacciones queda de la siguiente forma:
¿Se puede usar el paso h = 0.3? Si usamos un 0.3, de tamaño de paso, podemos observar incongruencias, esto es debido a que la aproximacion no es buena, da valores cada 0.3, por lo que produce un gran error. Usa como ordenada, el punto perteneciente a la recta tangente del anterior punto,por lo que la diferencia entre la ordenada real y la aproximada es notable.
No es recomendable entonces emplear un tamaño de paso tan amplio.
∂f/∂y=k_1 (〖-a〗_0 〖-b〗_0+2y)