Diferencia entre revisiones de «Reacciones Complejas Grupo11C»
| Línea 70: | Línea 70: | ||
}} | }} | ||
| − | [[Archivo:Ejercicio3_grafica.jpg|marco| | + | [[Archivo:Ejercicio3_grafica.jpg|marco|centro]] |
| Línea 101: | Línea 101: | ||
}} | }} | ||
| − | [[Archivo:Ejercicio4_grafica.jpg|marco| | + | [[Archivo:Ejercicio4_grafica.jpg|marco|centro]] |
== PVI con Trapecio y Runge-Kutta == | == PVI con Trapecio y Runge-Kutta == | ||
| Línea 109: | Línea 109: | ||
}} | }} | ||
| − | [[Archivo:Ejercicio5_grafica.jpg|marco| | + | [[Archivo:Ejercicio5_grafica.jpg|marco|centro]] |
== Reacción consecutiva: obtención de la ecuación diferencial y PVI == | == Reacción consecutiva: obtención de la ecuación diferencial y PVI == | ||
| Línea 129: | Línea 129: | ||
}} | }} | ||
| − | [[Archivo:Ejercicio7_01_grafica.jpg|marco| | + | [[Archivo:Ejercicio7_01_grafica.jpg|marco|centro]] |
| − | [[Archivo:Ejercicio7_03_grafica.jpg|marco| | + | [[Archivo:Ejercicio7_03_grafica.jpg|marco|centro]] |
== Resolución e interpretación del sistema por Euler y Runge-Kutta con k2=1/5 == | == Resolución e interpretación del sistema por Euler y Runge-Kutta con k2=1/5 == | ||
| Línea 141: | Línea 141: | ||
}} | }} | ||
| − | [[Archivo:Ejercicio8_grafica.jpg|marco| | + | [[Archivo:Ejercicio8_grafica.jpg|marco|centro]] |
[[Categoría:Ecuaciones Diferentiales]] | [[Categoría:Ecuaciones Diferentiales]] | ||
[[Categoría:ED14/15]] | [[Categoría:ED14/15]] | ||
[[Categoría:Trabajos 2014-15]] | [[Categoría:Trabajos 2014-15]] | ||
Revisión del 20:10 4 mar 2015
| Trabajo realizado por estudiantes | |
|---|---|
| Título | Reacciones complejas (Grupo 11C) |
| Asignatura | Ecuaciones Diferenciales |
| Curso | Curso 2014-15 |
| Autores |
Martín Salmerón, Carlos Molina de Francia, Víctor Pérez Abellán, Ignacio David Rueda, Juan Manuel Vallino, Carlos |
| Este artículo ha sido escrito por estudiantes como parte de su evaluación en la asignatura | |
Contenido
- 1 Introducción
- 2 Ecuación diferencial: validación e interpretación
- 3 ¿Cómo cambiaría la ecuación si el proceso fuera reversible?
- 4 PVI por Euler
- 5 Límite de las concentraciones
- 6 PVI con Trapecio y Runge-Kutta
- 7 Reacción consecutiva: obtención de la ecuación diferencial y PVI
- 8 Resolución e interpretación del sistema por Euler y Runge-Kutta con k2=5
- 9 Resolución e interpretación del sistema por Euler y Runge-Kutta con k2=1/5
1 Introducción
Consideramos una reacción química irreversible en una solución bien mezclada, suponiendo que la reacción ocurre a volumen y temperatura constantes y que cumple la ley de acción de masas. Ésta última nos indica la relación de proporcionalidad entre la velocidad de reacción y las concentraciones de los reactivos.
A + B → C
Como se puede observar, en nuestra reacción inicialmente intervienen dos reactivos A y B que forman un producto C mediante una reacción bimolecular, es decir, para formar una molécula de C hará falta una de A y una de B.
2 Ecuación diferencial: validación e interpretación
Supuesta la reacción bimolecular irreversible anteriormente mencionada y dado que se cumple la acción de masas, podemos establecer la ecuación diferencial:
y′(t)=k1(a0−y(t))(b0−y(t)) para t>0
Cuyos elementos podemos interpretar como:
.y′(t) velocidad de reacción a lo largo del tiempo.
.y(t) concentración del producto C a lo largo del tiempo.
.a0 es la concentración inicial del reactivo A.
.b0 será la concentración inicial de B.
.k1 es la constante específica de la velocidad de reacción, cuyas unidades se adaptan en base al número de reactivos [s^(-1)*mol^(1-n)*L^(n-1)], siendo n el número de reactivos.En nuestro caso, la condición de que la temperatura sea constante, implica que la constante específica de la velocidad de reacción es constante también.
Problema de valor inicial: Atendiendo al teorema de la existencia y unicidad de Cauchy, podemos asegurar que nuestra ecuación diferencial lo cumple, puesto que la función es continua en nuestro dominio (t>0), lo que implica que admite solución, y su primera derivada al ser también continua en su dominio, admitirá una única solución.
3 ¿Cómo cambiaría la ecuación si el proceso fuera reversible?
Dado que se sigue cumpliendo la ley de acción de masas, podemos relacionar las velocidades de reacción del proceso directo e inverso mediante sus respectivas constantes específicas de velocidad de reacción k1 y k2, obteniendo finalmente como ecuación diferencial para trabajar:
y'(t)=k1*(a0-y(t))*(b0-y(t))-k2*y(t)
Como comentario, podemos añadir que las constantes específicas de velocidad de reacción se relaciónan entre sí mediante la constante de equilibrio de la reacción K (K=k1/k2).
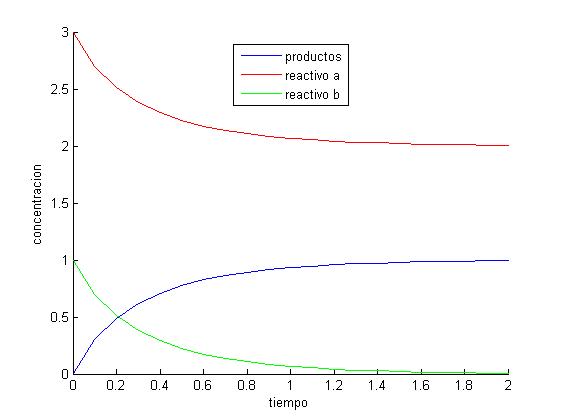
4 PVI por Euler
t0=0;
tN=2;
y0=0;
h=0.1;
N=round((tN-t0)/h);
t=t0:h:tN;
y=zeros(1,N+1);%euler
y(1)=y0;
for i=1:N
y(i+1)=y(i)+h*k1*(a0-y(i))*(b0-y(i))
end
%sacamos tabla de resultados
[t',y']
%gráfico
hold on
plot(t,y)
plot(t,(a0-y),'r')
plot(t,(b0-y),'g')
legend('productos','reactivo a','reactivo b','location','best');
xlabel('tiempo');
ylabel('concentracion');
hold off
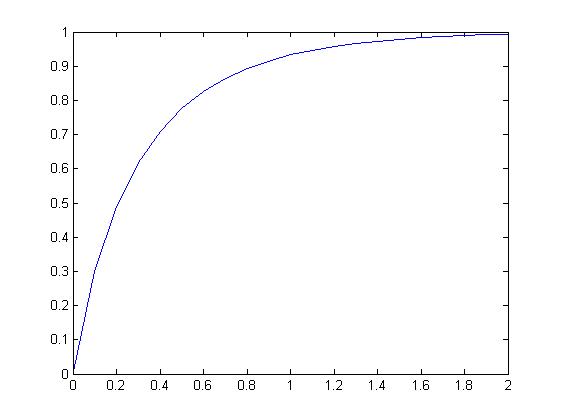
5 Límite de las concentraciones
%Hallamos el límite de la Ecuación Diferencial, y nos da 1, ya que la concentración final del elemento C debe ser el resultado de la concentración del reactivo limitante
%DATOS DEL PROBLEMA
t0=0;
y0=0;
h=0.1;
t(1)=t0;
y(1)=y0;
i=1;
%el límite es 1, el objetivo es alcanzar 1
%objetivo
lim=1;
while abs(lim-y(i))>1*lim
y(i+1)=y(i)+h*k1*(a0-y(i))*(b0-y(i)); %euler
t(i+1)=t(i)+h;
i=i+1;
end
[t',y']
disp('Tiempo final:')
disp(t(end))
plot(t,y)
%Vemos que cuando el tiempo es igual a 2, se puede aproximar al valor que obtendríamos para C con t=?
%Sí, es lógico lo que se observa, dado que como hemos visto en la gráfica
%del apartado anterior, la curva tiende a estabilizarse en el valor 1
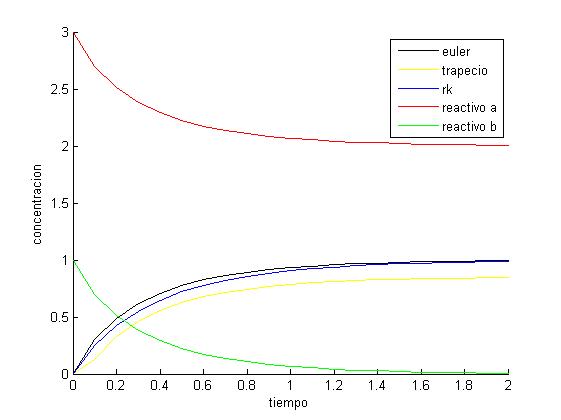
6 PVI con Trapecio y Runge-Kutta
7 Reacción consecutiva: obtención de la ecuación diferencial y PVI
Basándonos en la ley de acción de masas, y sabiendo que se produce la reacción consecutiva que se nos indica en el enunciado, podemos plantear un sistema con estas dos ecuaciones para obtener el PVI asociado.
y'1=k1*(a0-y1(i))*(b0-y1(i))
y'2=k2*(y1(i)-y2(i))
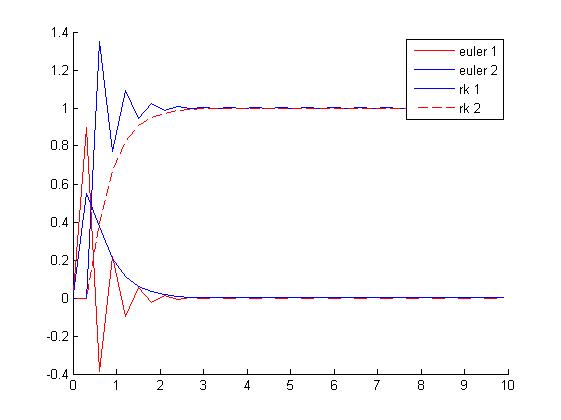
8 Resolución e interpretación del sistema por Euler y Runge-Kutta con k2=5
Haciendo uso del sistema de ecuaciones del apartado anterior; con los valores indicados en este apartado (k2=5, en los primeros 10 segundos y utilizando un paso de 0.1), y a través de los métodos de Euler y Runge-Kutta, podemos hacer una primera interpretación de la gráfica resultante. En el caso de realizar este ejercicio con un paso de 0.3, se puede observar como la gráfica se distorsiona, por lo cual llegamos a la conclusión que en los métodos utilizados, es preferible emplear pasos pequeños, dado que en los métodos explícitos con pasos grandes provocan que la gráfica se empiece a separar de la solución real.
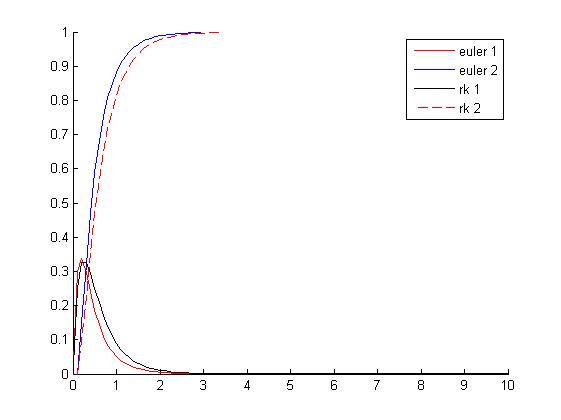
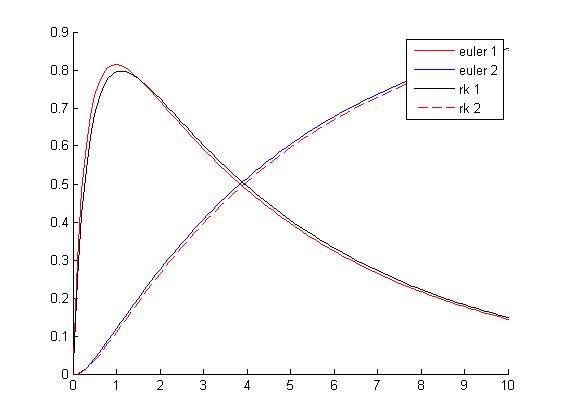
9 Resolución e interpretación del sistema por Euler y Runge-Kutta con k2=1/5
Haciendo uso del sistema de ecuaciones del apartado 6; con los valores indicados en este apartado (k2=1/5, en los primeros 10 segundos y utilizando un paso de 0.1) y a través de los métodos de Euler y Runge-Kutta, podemos hacer una primera interpretación de la gráfica resultante.