Diferencia entre revisiones de «Reacciones complejas - Grupo 16 A»
(→Resolución numérica cuando t→∞ [Apartado 4]) |
(→PVI con el método Euler [Apartado 3]) |
||
| Línea 82: | Línea 82: | ||
La gráfica obtenida es: | La gráfica obtenida es: | ||
| − | [[Archivo: | + | [[Archivo:Ap3_1fig.jpg|marco|izquierda]] |
Revisión del 14:58 2 mar 2015
| Trabajo realizado por estudiantes | |
|---|---|
| Título | Reacciones complejas. (Grupo 16-A) |
| Asignatura | Ecuaciones Diferenciales |
| Curso | Curso 2014-15 |
| Autores |
Arévalo Lecanda, Javier Buitrago Peña, Marcos Chamizo Carmona, Javier La Porta, Nicoletta |
| Este artículo ha sido escrito por estudiantes como parte de su evaluación en la asignatura | |
Contenido
- 1 Introducción
- 2 Problema de Valor Inicial (PVI) [Apartado 1]
- 3 Ecuación diferencial si el proceso es reversible [Apartado 2]
- 4 PVI con el método Euler [Apartado 3]
- 5 Resolución numérica cuando t→∞ [Apartado 4]
- 6 Resolución por los métodos del trapecio y de Runge Kutta [Apartado 5]
- 7 Sistema de dos ecuaciones diferenciales [Apartado 6]
- 8 Resolución numérica cuando k2=5 [Apartado 7]
- 9 Resolución numérica cuando k2=1/5 [Apartado 8]
1 Introducción
En este articulo vamos estudiar un ejercicio de modelización en el cual consideramos una reacción química irreversible en una solución bien mezclada. La reacción en cuestión es en una reacción bimolecular que consiste en que una molécula de A y una de B se juntan para crear una de C.
A + B → C
Para nuestro ejercicio, supondremos varias cosas:
- La reacción ocurre para un volumen constante.
- La reacción ocurre para una temperatura constante.
- La reacción satisface la ley de acción de masas que establece que la velocidad de reacción es proporcional al producto de las concentraciones de los reactivos (A y B)
2 Problema de Valor Inicial (PVI) [Apartado 1]
Lo primero que debemos hacer para resolver este problema es pasar el fenómeno químico a un problema de valor inicial. Para eso usamos la ley de acción de masas.
En esta ecuación tendremos varias constantes
- k1: Esta contante es la que nos da la proporcionalidad de la reacción.
- a0: Esta constante es la que determina la concentración inicial de A.
- b0: Esta constante es la que determina la concentración inicial de B.
Ademas de estas constantes tendremos también las variables:
- y(t): Esta variable nos da la concentración de C respecto al tiempo.
- y'(t): Es la derivada de y(t) respecto al tiempo.
Tenemos también que mencionar la concentración de A respecto al tiempo que sera (a0−y(t)) y la de B que sera (b0−y(t)). Para nuestra ecuación tomaremos el tiempo como estrictamente mayor que 0: t>0.
Podemos entonces deducir que la ecuación sera:
y′(t)=k1(a0−y(t))(b0−y(t))
3 Ecuación diferencial si el proceso es reversible [Apartado 2]
Hasta ahora hemos supuesto que el proceso no era reversible, esto significa que A y B se juntaban para crear C. Si ahora suponemos que el proceso es reversible, ademas de A y B juntándose para crear C también tendremos C descomponiéndose para formar A y B. La ecuación diferencial se veria afectada por este cambio.
Tendríamos que añadir nuevos parámetros:
- k2: Ademas de tener k1, necesitaremos también conocer k2 que es la proporcionalidad de la reacción reversible.
- c0: Esta constante es la que determina la concentración inicial de C.
Ahora solo tendríamos que reescribir la ecuación diferencial anterior restando le la descomposición de C en A y B.
y′(t)=k1(a0−y(t))(b0−y(t))−k2(c1+y(t))
4 PVI con el método Euler [Apartado 3]
Vamos ahora a resolver el problema de valor inicial numéricamente con el método de Euler, de aquí en adelante tomaremos la reacción como irreversible.
Primero damos valores a nuestros parametros según el enunciado del trabajo:
- a0=3 mol/l
- b0=1 mol/l
- k1=1 mol/s
- h=0.1
- t: [0,2]
Nuestro codigo sera:
a0=3; b0=1; %Concentraciones iniciales de A y B
t0=0; tf=2; %Tiempos iniciales y finales
y0=0; %Tomamos la concentracion de C inicial como 0
k1=1;
h=0.1; %Paso
N=(tf-t0)/h;
t=t0:h:tf;
y=zeros(1,N+1);
yy=y0;
for n=1:N
yy=yy+h*(k1*(a0-yy)*(b0-yy));
y(n+1)=yy;
end
A=a0-y; %Concentracion de A
B=b0-y; %Concentracion de B
hold on
plot(t,y,'r')
plot(t,A,'b')
plot(t,B,'g')
legend('C','B','A')
hold off
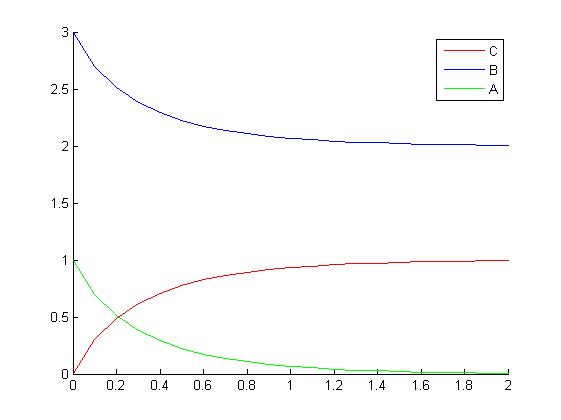
La gráfica obtenida es:
En este gráfico tenemos: la concentración de A en azul, la concentración de B en verde y la concentración de C en rojo. Se puede apreciar fácilmente lo que ocurre en la reacción, las concentraciones de A y de B disminuyen en el tiempo a la misma velocidad en la que la concentración de C crece. Podemos también observar que el limitante en esta reaccion es el B.
5 Resolución numérica cuando t→∞ [Apartado 4]
Como no podemos operar con t=∞ debemos para el programa cuando el valor de las concentraciones se vuelva constante y la velocidad de reacción sea cero, como nuestra reaccíon es irreversible ésta terminará en el momento en que se acabe el reactivo limitante.