Diferencia entre revisiones de «Reacciones complejas. (Grupo A8)»
(→Método de Euler) |
(→Casos prácticos. Aplicación del análisis numérico.) |
||
| Línea 41: | Línea 41: | ||
*<math>k_1=1</math> | *<math>k_1=1</math> | ||
| − | *<math>a_0=3</math> | + | *<math>a_0=3 mol/l</math> |
| − | *<math>b_0= | + | *<math>b_0=1mol/l</math> |
Entrando con estos valores en la ecuación diferencial, nos queda:: | Entrando con estos valores en la ecuación diferencial, nos queda:: | ||
Revisión del 11:53 24 feb 2015
| Trabajo realizado por estudiantes | |
|---|---|
| Título | Reacciones complejas (Grupo A8) |
| Asignatura | Ecuaciones Diferenciales |
| Curso | Curso 2014-15 |
| Autores | Valentina Salazar; Antonio Carrero; Juan José Hernandez; José Francisco Aguilera |
| Este artículo ha sido escrito por estudiantes como parte de su evaluación en la asignatura | |
Contenido
1 Introducción y modelización del problema.
En este artículo vamos a examinar el comportamiento cinético de las reacciones químicas, estudiaremos mediante análisis numérico las reacciones químicas irreversibles y nos limitaremos a plantear una suposición teórica del comportamiento de las las reacciones reversibles.
Para realizar este estudio, formularemos las siguientes hipótesis sobre las condiciones y el comportamiento de las reacciones químicas:
- Los componentes de la reacción química se considerarán perfectamente mezclados.
- La reacción química se realiza en condiciones de volumen y temperatura constantes.
- Consideraremos la reacción química que planteamos perfectamente ajustada.
- Suponemos que para el instante [math]t=0[/math] la concentración de producto es nula.
Partiendo de estas hipótesis y suposiciones sobre las reacciones que vamos a estudiar, consideraremos el proceso químico:: [math]{A+B}\Rightarrow{C}[/math]
Siendo esta una reacción bimolecular, en la que los reactivos [math]A[/math] y [math]B[/math] interaccionan formando un producto [math]C[/math]. Regiremos nuestro estudio cinético de esta reacción por la ley de acción de masas, que establece que la velocidad de reacción es proporcional al producto de las concentraciones de los reactivos. Siguiendo esta ley podemos deducir la siguiente ecuación diferencial que nos define las cantidades de producto y reactivos a lo largo del tiempo::
[math]y'(t)=k_1(a_0-y(t))(b_0-y(t))[/math]
Donde:
- [math]y(t)[/math] nos define como evoluciona la concentración de producto [math]C[/math] a lo largo del tiempo.
- [math]y'(t)[/math] es la derivada de la concentración de [math]C[/math] con respecto al tiempo.
- [math]a_0[/math] indica la concentración inicial de producto [math]A[/math].
- [math]b_0[/math] indica la concentración inicial de producto [math]B[/math].
- [math]k_1[/math] representa la constante de proporcionalidad de la reacción.
Podemos comprobar que al estar la estequiometría de la reacción ajustada podemos decir que para una concentración [math]y(t)[/math] en cada instante de tiempo [math]t[/math], tendremos concentraciones [math]a_0-y(t)[/math] y [math]b_0-y(t)[/math] de [math]A[/math] y [math]B[/math] respectivamente. Entonces si la velocidad de reacción, [math]y'(t)[/math], es directamente proporcional a la concentración de los reactivos, suponiendo una constante de proporcionalidad [math]k_1[/math] y una concentración inicial nula de producto para [math]t=0[/math], siguiendo la ley de acción de masas nos lleva a la ecuación predicha anteriormente::
[math]y'(t)=k_1(a_0-y(t))(b_0-y(t))[/math]
Partiendo de esta ecuación podemos empezar a hacer análisis numérico del proceso.
2 Proceso reversible.
En el caso de suponer un proceso químico reversible veríamos afectada la ecuación diferencial que nos cuantifica la concentración de producto en un término reductor de esta, que nos representaría la velocidad de formación de reactivos, proporcional a la concentración actual de producto por otra constante de proporcionalidad diferente [math]k_2[/math].:
[math]y'(t)=k_1(a_0-y(t))(b_0-y(t))-k_2(y(t))[/math]
3 Casos prácticos. Aplicación del análisis numérico.
Para realizar el análisis numérico del proceso, cuantificaremos las constantes que dan forma a la ecuación cinética:
- [math]k_1=1[/math]
- [math]a_0=3 mol/l[/math]
- [math]b_0=1mol/l[/math]
Entrando con estos valores en la ecuación diferencial, nos queda::
[math]y'(t)=(3-y(t))(1-y(t))[/math]
Que modelizaremos siguiendo los métodos numéricos de Euler, trapecio y Runge-Kutta.
3.1 Método de Euler
Implementamos este modelo introduciendo el siguiente código en Octave:
t0=0;
tN=4; % Initial and final times
y0=0; % Initial data
N=40;
h=(tN-t0)/40; % Discretization
t=t0:h:tN; % time vector
y=zeros(1,N+1); % solution vector y
y(1)=y0; % save solution at time t0; y(1)
a0=3;
b0=1;
yy=y0; % computing variable yy
for n=1:N
yy=yy+h*(a0-yy)*(b0-yy); % compute y(n + 1) from y(n)
y(n+1)=yy; % save y(n + 1)
end
A=a0.-y;
B=b0.-y;
plot(t,y)
hold on
plot(t,A,'r')
hold on
plot(t,B,'y')
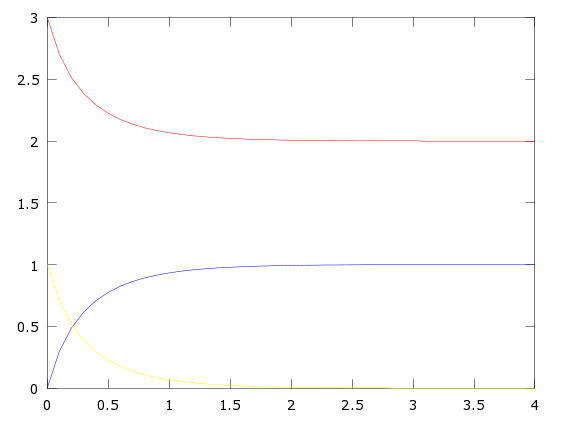
Mediante este código obtenemos la gráfica de las concentraciones de los reactivos y productos, que se muestra en la siguiente imagen:
Como podemos ver en la imagen la concentración de los reactivos y productos se vuelve asintótica tendiendo la de [math]A=2 mol/l[/math], la de [math]B=0 mol/l[/math] y la de [math]C=1 mol/l[/math]. Lo que por la estequiometría de la reacción es lógico, ya que el producto [math]C[/math] dejará de formarse cuando se agote uno de los dos reactivos que lo forman; en nuestro caso disminuye progresivamente la concentración de [math]B[/math] y a la vez se estabilizan las concentraciones, ya que se reduce la velocidad de reacción [math]y'(t)[/math].